研究紹介
創薬薬理学の研究について
タンパク質分解機構の生理機能解明とタンパク質分解誘導薬物の開発を細胞レベルから個体レベルで取り組みます。病態発症メカニズムを分子レベルで理解し、創薬のターゲットと作用薬物を提示することを目指します。生化学・分子生物学的な手法を駆使し、ゲノム編集技術により作成したマウスを利用して、目標を達成していきます。
ユビキチンリガーゼの生理機能と創薬
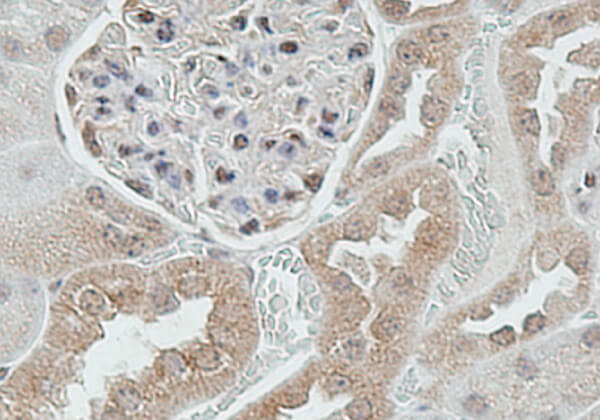
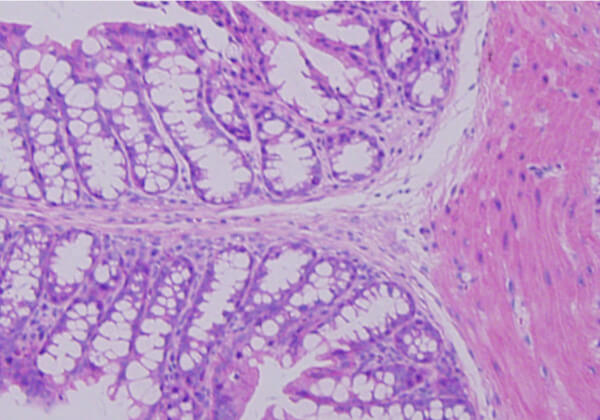
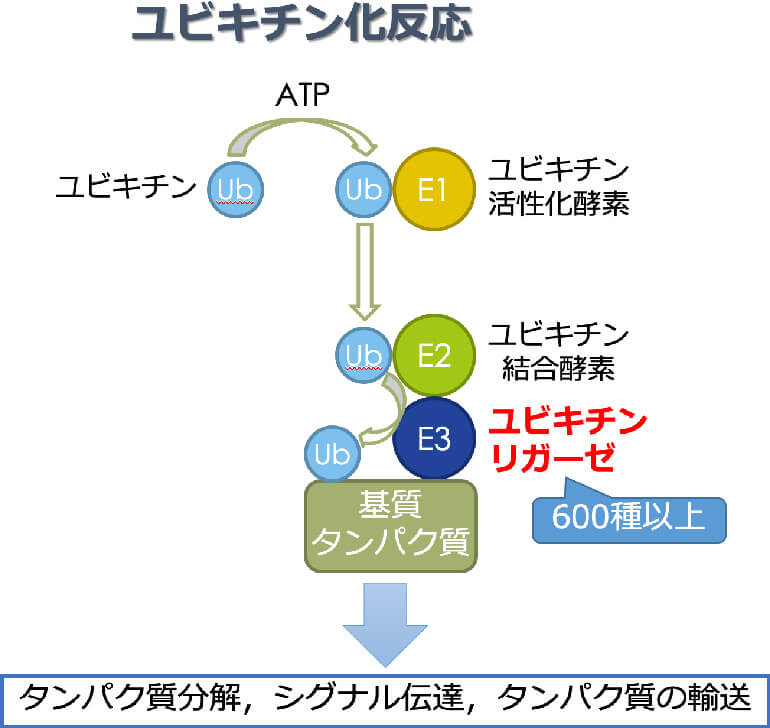
ユビキチン(Ub)は76個のアミノ酸からなる小さなタンパク質ですが、細胞内においてタンパク質のリジン残基に共有結合することで様々な生命機能(タンパク質分解・シグナル伝達・タンパク質輸送など)に関与しています。ユビキチンの基質タンパク質への修飾(ユビキチン化)を触媒する3つの酵素群がありますが、その中でユビキチンリガーゼ(E3)は基質の特異性と反応速度を規定する最も重要な酵素です。その数は600種以上あると推測されていますが、その機能に関しては不明なものが多く存在しています。私たちはこれまで新規のユビキチンリガーゼを同定し、その生理機能と疾患への関与に取り組んできました。アルツハイマー病や炎症性腸疾患などに関連するユビキチンリガーゼをこれまで見出してきましたが、今後はユビキチン化に関連した創薬にも挑戦していきます。
ユビキチンリガーゼの生理機能と疾患への関与
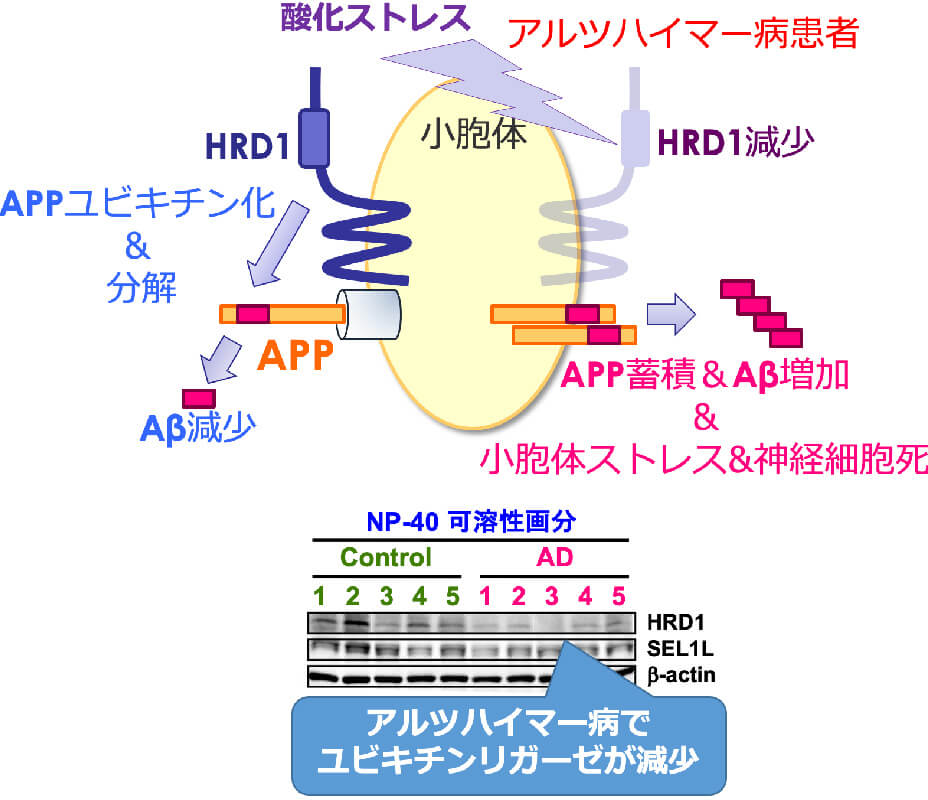
ゲノム編集を用いた遺伝子の機能解析
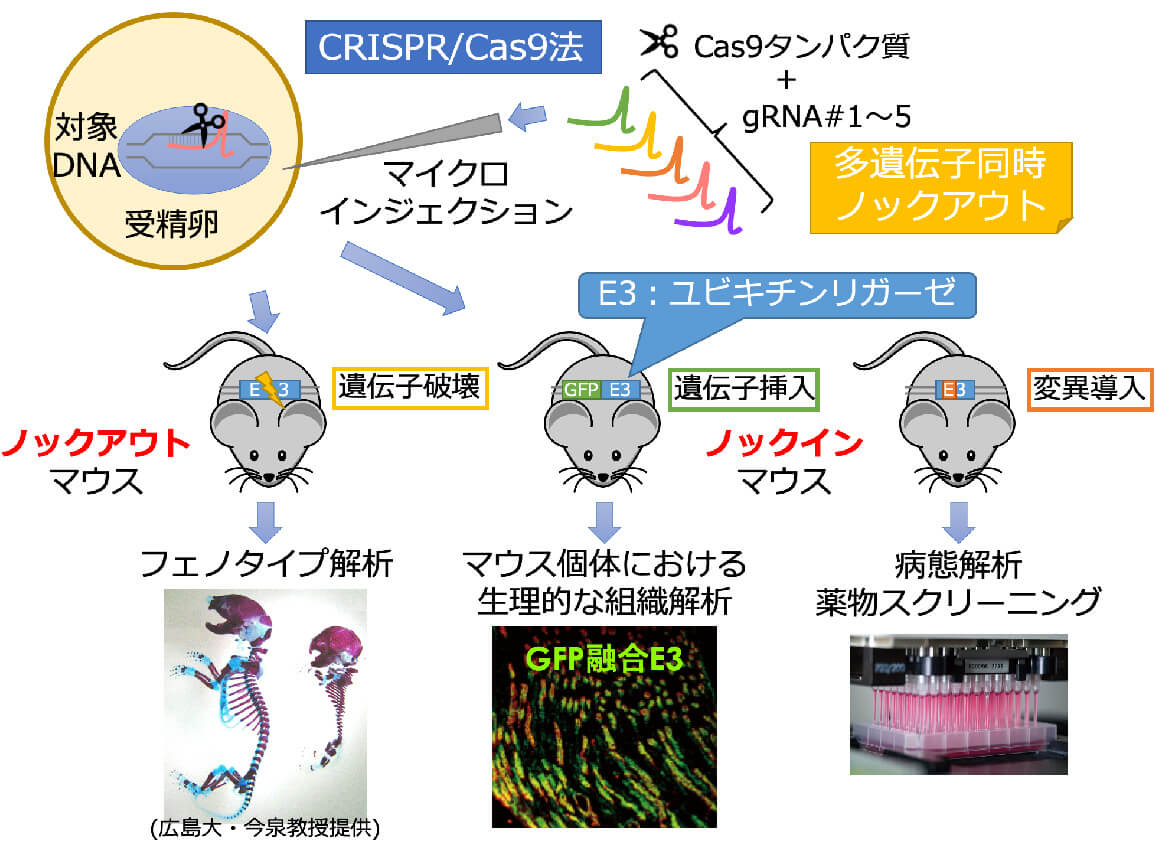
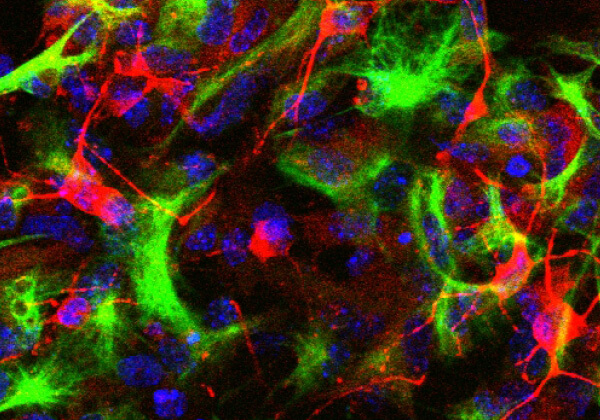
ゲノム編集は2013年にCRISPR/Cas9システムが開発されると急速に普及し、瞬く間に2020年のノーベル化学賞受賞研究となりました。それ程インパクトのあるツールであることを証明しています。私たちはこれまでCRISPR/Cas9システムを用いて、ノックアウト(遺伝子破壊)およびノックイン(遺伝子挿入)を細胞やマウスで行ってきました。特にCRISPR/Cas9システムによってハードルが下がったノックイン技術は強力なツールになるため、今後は様々な機能を持った遺伝子を研究対象の遺伝子に挿入することで、生理的発現レベルの遺伝子産物を細胞やマウスを用いて解析していきたいと思います。